Специфическую форму гломерулонефрита представляет собой синдром Берже. Инфекционно-аутоиммунную почечную патологию называют идиопатической возвратной, фокальной или синфарингитной макрогематурией. Развитие болезни провоцирует повышенная концентрация lgA-комплексов в субэндотелиальных тканях.
Причины
Такую форму гломерулонефрита характеризует сложная, многофакторная этиология с инфекционным, иммунологическим, генетическим триггерным спусковыми механизмом либо их сочетанием. Единственная причина очагово-диффузной пролиферации мезангиальных клеток не определена.

Болезнь Берже имеет клинически подтвержденную связь с:
- бактериальными агентами;
- вирусными возбудителями;
- хромосомными мутациями;
- аутоиммунными патологиями.
Значение наследственных факторов в развитии очагово-пролиферативного гломерулонефрита косвенно доказывает расово-этническое распространение патологии. В азиатских странах заболевание встречается в 5-6 раз чаще, чем в европейских и латиноамериканских.
Связь с инфекционными поражениями подтверждают сезонные вспышки. В осенне-зимний период наблюдается увеличение частоты клинически фиксируемых случаев идиопатической возвратной макрогематурии, что объясняется эпидемиологическими причинами.
Факторы развития очагов-пролиферативного гломерулонефрита:
- Инфекционные. Заболевание провоцируют типичные бактериальные или вирусные возбудители воспалительных процессов дыхательной системы, желудочно-кишечного тракта, кожного покрова. Поражение почечного аппарата связывают с агрессивной защитной реакцией организма на инфекционное вторжение.
- Иммунологические. Развитию почечного заболевания способствует интенсивный синтез lgA-комплексов, не подающихся быстрой элиминации – выведению нефротическим или гепатобилиарным путем. В результате биохимически и физиологически активные соединения аккумулируются в мезангиальных тканях.
- Аллергенные. В качестве триггерных факторов выступают биологически чужеродные частицы любого происхождения. Неадекватную реакцию иммунной системы с усиленной выработкой lgA-комплексов провоцируют химические реагенты, продукты цветения, бытовые химикаты, промышленные испарения.
- Наследственные. Соответствующие исследования демонстрируют наличие у большинства пациентов с идиопатической возвратной макрогематурией нетипичных мутаций в 6-й хромосомной паре, аномальные изменения в ответственном за контроль синтеза рецепторов гепатоцитов участке генной цепи.

Указанные факторы – предмет научно-медицинских дискуссий. Предположительно они выступают причиной полиморфной клинической картины заболевания. К факторам риска причисляют паразитарные инвазии, чрезмерное употребление насыщенных казеином и глютеном пищевых продуктов, гормонально-зависимые опухолевые процессы.
Патогенез
Основным научно доказанным сценарием развития такой формы гломерулонефрита считается образование в крови иммунных комплексов с содержанием полимерной разновидности глобулина класса А.
В норме физиологически малозначимые концентрации указанных веществ содержат:
- эпителий внутренних органов;
- слизистое покрытие верхних отделов дыхательного тракта;
- лимфатический секрет;
- гематологическая жидкость.
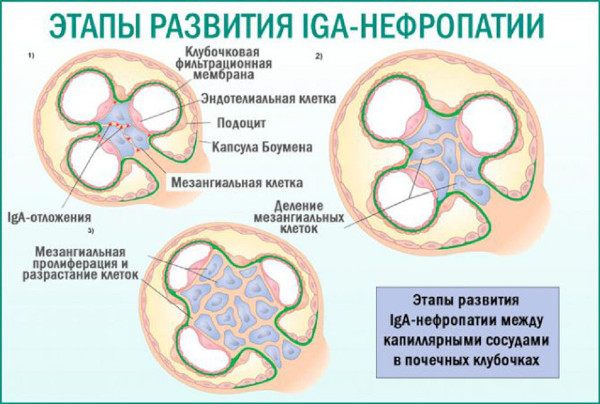
Патогенез очагово-пролиферативного гломерулонефрита обусловлен аномалиями синтеза lgA-комплексов в костном мозге под воздействием представленных выше триггерных факторов. Накопительный эффект усиливают нарушения в рецепторах клеток печени и почек, препятствующие выведению иммунокомпетентных соединений.
В результате крупные молекулы полимерных глобулинов сосредоточиваются в клубочках нефронов. Отложения физиологически активного вещества приводят в действие лейкоцитарные реакции с системой комплимента – сочетанием кровяных белков и протеолитических ферментов, ответственных за формирование гуморального иммунитета.
Результатом патогенетического каскада становится вялотекущий воспалительный процесс диффузного типа в нефротическом механизме, характеризуемый повышенным содержанием в мочевых выделениях:
- эритроцитарных тел;
- альбуминов – основных белковых фракций крови;
- частиц отслоившегося эпителия;
- некротизированных фрагментов паренхиматозной оболочки.
Болезнь Берже связана с нарушенным клиренсом иммунных комплексов. Основным патогенетическим фактором такого состояния считается аномальная экспрессия расположенного на мембранах гепатоцитов асиаглогликопротеинового рецептора ASGPR, предназначенного для распознавания галактозы и катаболизации соединения lgA.
По происхождению, набору симптоматических признаков, тяжести протекания выделяют представленные в таблице формы аутоиммунного гломерулонефрита:
| Разновидность | Патогенетические характеристики |
| Идиопатическая | Самый распространенный вариант воспалительного заболевания почек сопряжен с гиперактивным синтезом глобулинов слизистыми клетками пищеварительных органов, респираторных каналов. |
| Вторичная | Служит частым осложнением глютеновой энтеропатии, ревматического процесса в суставных капсулах, саркаидоза – доброкачественного гранулематоза, поражающего мезенхиму с лимфатическими тканями. Вторичная форма lgA-нефропатии нередко сопровождает иммуннодефицит, гепатит В, кишечные воспаления. |
| Синфарингитная | Такая разновидность очагово-пролиферативного гломерулонефрита ассоциирована с инфекционными поражениями и склонна к обострениям в периоды напряженной эпидемиологической ситуации. Служит осложнением ларингита, фарингита, ангины. |
| Латентная | Самая опасная и труднодиагностируемая форма почечного заболевания. Хроническое протекание способно спровоцировать острую функциональную недостаточность фильтрующего органа. |
Наиболее редко возникающей и тяжелой считается нефротическая разновидность аутоиммунного поражения. Характеризуется обширным диффузным воспалением, имеет преимущественно вторичное происхождение.
Симптоматика и клиническая картина
Проявления аутоиммунного гломерулонефрита разнообразны и зависят от формы.
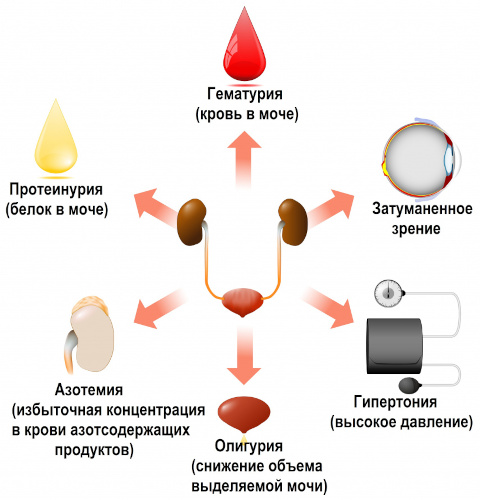
Для синфарингитной разновидности характерны симптомы в виде:
- дискомфортных или болезненных ощущений в пояснично-крестцовой зоне;
- красноватого цвета мочевых выделений из-за содержания кровянистых фрагментов;
- уменьшения суточного объема урины;
- роста показателя артериального давления;
- нарушенного водно-солевого равновесия.
Клиническую картину усугубляют недавно проведенная вакцинация, чрезмерное физическое напряжение, продолжительные инсоляции. У некоторых пациентов возникают сложности с мочеиспусканием.
Латентная форма lgA-нефропатии отличается бессимптомным протеканием со стороны почечного механизма. Заболевание определяют исключительно методами лабораторной диагностики.
Клинической картине свойственны:
- артралгические проявления;
- низкоинтенсивные мышечные боли;
- отеки мягких тканей лица и конечностей;
- вазоспастические признаки с нарушением артериального кровообращения в стопах и запястьях.
Самая выраженная клиническая картина присуща нефротическому варианту аутоиммунного гломерулонефрита. Симптоматический комплекс сочетает асцит с дегидратацией и признаками генерализованного отека подкожной клетчатки.
Методы диагностики
Болезнь почек идентифицируют на основании объективных клинико-лабораторных показателей. Инструментальные обследования при синдроме Берже носят вспомогательный и неспецифический характер. Ниже представлены применяемые методы диагностики.
Биопсия почки
Забор образца органических тканей необходим для выявления злокачественных изменений, назначения генетически обоснованного лечения. Процедуру проводят с помощью пункционной иглы или высокоскоростного медицинского пистолета.
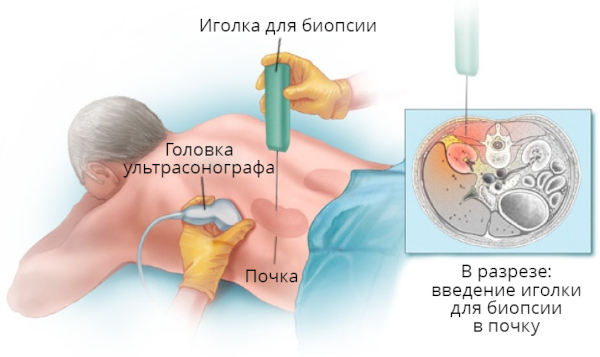
Морфологическое исследование полученного биоптата позволяет определить этиологические факторы развития воспалительного процесса. Процедуру выполняют только в тех случаях, когда неинвазивные методы не дают возможности окончательно верифицировать диагноз.
Гистологическому изучению подлежат кора органа, паренхиматозная оболочка. Методика позволяет уточнить степень активности воспалительного процесса, глубину диффузного проникновения, обширность очага поражения. Стоимость процедуры под контролем ультразвуковой аппаратуры – 4 650 руб.
Микроскопия
Таким способом изучают полученный образец органических тканей. При lgA-нефропатии показано выполнение оптической микроскопии. Техника заключается в применении увеличивающих линз с пропусканием через изучаемый образец световых волн видимого спектра.
О развитии аутоиммунного гломерулонефрита свидетельствует визуально фиксируемое повышение концентрации внеклеточного матрикса в мезангиальных тканях, составляющих серединную часть механизма кровоснабжения паренхиматозной оболочки. Стоимость процедуры в коммерческой клинике – 3500 руб.
Лабораторные анализы
В диагностический комплекс входят общеклиническое исследование мочи и биохимический тест крови.

Последний в фазе обострения заболевания демонстрирует:
- увеличение скорости оседания эритроцитов;
- умеренно выраженный лейкоцитоз – с содержанием иммунных клеток выше 9 000 единиц в 1 мкл исследуемого образца биологического материала;
- повышенную концентрацию гематокрита – соотношения форменных элементов к общему объему крови;
- избыточное насыщение гематологической жидкости глобулинами класса lgA;
- повышение содержания креатинина, сигнализирующее о нарушенных функциях механизма клубочной фильтрации.
При нефротической форме заболевания биохимический тест крови показывает сочетание гипоальбунемии с гиперлипедемией – сниженное и повышенное содержание белковых фракций с жировыми фрагментами соответственно.
Лабораторное исследование мочевых выделений у пациентов с синфарингитной разновидностью аутоиммунного воспаления почек фиксирует кровяные частицы, избыточное насыщение биологического материала протеиновыми белками свыше 2 г/л.
Инструментальные обследования
Стандартно назначают акустическое сканирование фильтрующего органа. Ультразвуковое обследование на начальной стадии заболевания или при латентной форме аутоиммунного воспаления не выявляет специфические изменения в конфигурации, расположении, размерах органа.
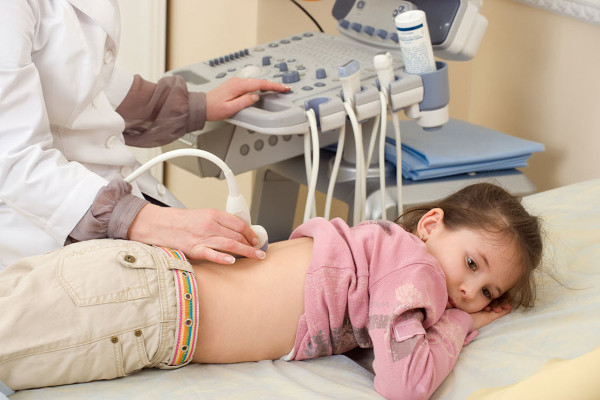
Такая диагностика имеет преимущественно дифференциальное предназначение. Для получения детальной и всеобъемлющей картины применяют экскреторную урографию с контрастным веществом. Заметна задержка введенного сульфата бария из-за нарушения фильтрующей функции почек.
Методы лечения
Болезнь Берже – аутоиммунное воспаление нефротического аппарата, требующее комплексной симптоматической терапии. Специфические методы этиотропного лечения не разработаны.
Комплексный подход предусматривает сочетание:
- противовоспалительных нестероидных средств;
- гормональных лекарств с иммуносупрессивными свойствами;
- нефропротекторных медикаментов;
- препаратов витаминной поддержки.
При развитии функциональной недостаточности органа показаны процедуры гемодиализа – внепочечной фильтрации крови с помощью специализированной медицинской аппаратуры.
При невозможности восстановления нефротического механизма выполняют трансплантацию. Такая хирургическая процедура применяется в исключительных случаях для продления жизни, но не считается эффективным методом лечения.
У 45-50% пациентов, перенесших операцию по замене собственного органа донорским, со временем развиваются аналогичные аутоиммунные процессы из-за экстраренального происхождения заболевания. Ниже представлены методы лечения лекарственными средствами.
Неиммуносупрессивная терапия
Назначают препараты для стабилизации сосудистого давления.
В рамках комплексной неиммуносупрессивной медикаментозной терапии применяют инъекционное введение или пероральный прием средств устранения артериальной гипертензии:
- Аккузида – комбинированного гипотензивного лекарства, повышающего выработку альдостерона, контролирующего тонус сосудистых стенок, уменьшающего потерю ионов калия;
- Вазотенза, содержащего синтетическое вещество, антагонистическое к рецепторам ангиотензина II;
- Вальсакора с тиазидным диуретиком в составе;
- Гизаара, не оказывающего физиологически значимого влияния на частоту сокращений сердечной мышцы, а избирательно воздействующего только на почечный аппарат.
Указанные фармацевтические продукты сочетают при неиммунносупрессивном лечении с ингибиторами ангиотензинпревращающего фермента – Периндоприлом, Рамиприлом или Беназеприлом. Такая лекарственная комбинация обеспечивает стойкий гипотензивный эффект.
В рамках поддерживающей нефропротекторной терапии используют антиагрегантные средства. Пациентам с любой формой аутоиммунного воспаления почек стандартно назначают Дипирамидол, обладающий выраженными антитромботическими свойствами.
При установленном лабораторными методами участии в развитии очагово-пролиферативного гломерулонефрита бактериальных возбудителей назначают антибиотики с учетом чувствительности штамма.
Иммунодепрессивная терапия
Болезнь Берже требует применения в комплексном лечении препаратов, снижающих выработку lgA-комплексов. Иммунные супрессоры показаны при тяжелом протекании воспалительного процесса.
В рамках такой терапии глюкокортикостероиды на основе метилпреднизолона или аналога сочетают с цитостатическими лекарственными средствами.
Дозировку и кратность применения профильный медицинский специалист подбирает индивидуально с учетом:
- формы заболевания;
- обширности воспалительного процесса;
- личной переносимости пациентом;
- выраженности протеинурии, отражающей степень повреждения почечного механизма;
- особенностей наблюдаемой клинической картины;
- наличия сопутствующих системных патологий.
Иммуносупрессивные средства не назначают при изолированной или спровоцированной болезнетворными возбудителями синфарингитной форме. В таких случаях соответствующие препараты неэффективны.
При выраженной динамике прогрессирования почечного воспаления с сохраненными или умеренно сниженными фильтрующими функциями органа назначают глюкокортикостероиды в таблетках на протяжении 3-5 дней с последующей диагностической оценкой достигнутого результата.
Прогноз
Исход варьируется в зависимости от разновидности заболевания, своевременности лечения, физиологических особенностей пациента. При длительном протекании воспалительного процесса в 30-50% случаев развивается хроническая почечная недостаточность с медленным и доброкачественным прогрессированием.
Самым благоприятным прогнозом отличается идиопатическая форма аутоиммунного гломерулонефрита.
К ухудшающим исход заболевания факторам причисляют:
- мужской пол;
- пожилой возраст;
- насыщенность сывороточной фракции крови креатинином свыше 150 мкмоль/л;
- хроническую артериальную гипертензию;
- выраженную гематурию;
- сопутствующие метаболические расстройства.
Шансы на благоприятный исход аутоиммунного гломерулонефрита повышают своевременное лечение инфекционных поражений дыхательных путей, желудочно-кишечного тракта, мочеполовой системы.
Возможные последствия и осложнения
Хронической функциональной недостаточности почек свойственно медленное, но неуклонное прогрессирование – на протяжении 10-15 лет с постепенным ухудшением соматического состояния пациента и лабораторных показателей. Грозным осложнением считается гиповолемический шок с быстрым уменьшением объема циркулирующей крови.

При таком последствии почечного воспаления возникают:
- сильное снижение артериального давления;
- эпизодические головокружения;
- тахикардическая симптоматика;
- периодические обморочные состояния.
К распространенным осложнениям относят нефротический криз, содержащий комплекс различных по клиническим характеристикам симптомов – массивную протеинурию, нарушение липидно-белкового обмена, отеки мягких тканей.
При злокачественном протекании lgA-нефропатии нередко возникает острый тромбоз периферических сосудов или проходящих через орган магистральных артерий. Выраженность осложнений при таком протекании заболевания зависит от адекватности лечения и компенсаторных возможностей организма.
Аутоиммунное поражение почечного аппарата чаще всего фиксируют у пациентов мужского пола возрастом до 30 лет. Болезнь отличается многофакторным патогенезом. Для инфекционного синдрома Бержа характерны сезонные обострения.
Видео о болезни Берже
Дифференциальная диагностика болезни Берже:
